Иприт, бис (2-хлороетил) сульфид — сульфуроорганична соединение состава (ClCH 2 CH 2)2 S. Иприт впервые был получен немецким химиком Виктором Меером в 1886 году. Этому предшествовали работы химиков Деспре (1822), Немана (1859), Гутмана (1860), которые исследовали данный класс соединений, однако не выделили ее в чистом виде.
Чистый иприт представляет собой бесцветную маслянистую веществом без запаха (технический иприт имеет чесночно-горчичный запах и желто-коричневый цвет). Плохо растворяется в воде и неограниченно — во многих органических растворителях.
Во времена Первой мировой войны иприт применялся как боевое отравляющее вещество кожно-нарывного действия. Международное обозначение иприта как химического оружия — HD. Боеприпасы с ипритом в Германии сказывались желтым крестом (он входит в состав боевой смеси желтый крест, нем. Gelbkreuz), в США кодируются двумя зелеными кольцами.
В 1993 году, в результате подписания Конвенции о химическом оружии, использование иприта как химического оружия было запрещено. Его включили в список 1, который регламентирует производство и оборот опасных веществ.
Срок иприт происходит от названия бельгийского города Ипр, вблизи которого в ночь на 13 июля 1917 немецкими войсками впервые применен данное вещество как химическое оружие.
Токсическое действие иприта заключается в повреждении глаз, кожи, дыхательных путей. Симптомы отравления проявляются со скрытым периодом в 2:00, но при жаркой погоде и влажной кожи они появляются сразу. Следствием контакта с веществом появление пузырьки с желтоватой жидкостью, которые долго заживают и оставляют рубцы. При концентрации иприта в воздухе 0,03 мг / л смерть наступает в течение 2-5 минут.
Вещество быстро проникает в строительные материалы, поглощается текстилем, резиной, бумагой, поэтому отравления возможно и при контакте с зараженными предметами.
История[ | ]
Был синтезирован Сезаром Депре (англ.) в 1822 году и (независимо) британским учёным Фредериком Гутри (англ.) в 1860 году[1].
Первоначально веществу было присвоено название Lost — сокращение от фамилий учёных Wilhelm Lommel и Wilhelm Steinkopf[en], создавших в 1916 году метод его выработки в промышленных масштабах для Германской имперской армии[2].
Впервые иприт был применён Германией 12 июля 1917 года против англо-французских войск, которые были обстреляны минами, содержавшими маслянистую жидкость, у бельгийского города Ипра (откуда и произошло название этого вещества)[3].
Кроме того, иприт применялся в итало-эфиопскую войну 1935—1936 годов.
В декабре 1943 года в результате бомбардировки города Бари немецкой авиацией был потоплен американский транспорт «Джон Харви», перевозивший бомбы с ипритом. В результате утечки газа большое количество американских моряков и местных жителей получили отравления, в том числе со смертельным исходом[4].
История
Был синтезирован Сезаром Депре (англ.) в 1822 году и (независимо) британским учёным Фредериком Гутри (англ.) в 1860 году[1].
Первоначально веществу было присвоено название Lost — сокращение от фамилий учёных Wilhelm Lommel и Wilhelm Steinkopf[en], создавших в 1916 году метод его выработки в промышленных масштабах для Германской имперской армии[2].
Впервые иприт был применён Германией 12 июля 1917 года против англо-французских войск, которые были обстреляны минами, содержавшими маслянистую жидкость, у бельгийского города Ипра (откуда и произошло название этого вещества)[3].
Кроме того, иприт применялся в итало-эфиопскую войну 1935—1936 годов.
В декабре 1943 года в результате бомбардировки города Бари немецкой авиацией был потоплен американский транспорт «Джон Харви», перевозивший бомбы с ипритом. В результате утечки газа большое количество американских моряков и местных жителей получили отравления, в том числе со смертельным исходом[4].
Получение[ | ]
Иприт получают тремя способами:
- Из этилена и хлоридов серы, например S2Cl2 или SCl2:
2 C H 2 = C H 2 + S C l 2 → ( C H 2 C l — C H 2 ) 2 S {\displaystyle {\mathsf {2CH_{2}{\text{=}}CH_{2}+SCl_{2}\rightarrow (CH_{2}Cl{\text{-}}CH_{2})_{2}S}}}
- Из тиодигликоля S(CH2CH2OH)2 и трихлорида фосфора PCl3:
3 ( H O — C H 2 — C H 2 ) 2 S + 2 P C l 3 → 3 ( C H 2 C l — C H 2 ) 2 S + 2 H 3 P O 3 {\displaystyle {\mathsf {3(HO{\text{-}}CH_{2}{\text{-}}CH_{2})_{2}S+2PCl_{3}\rightarrow 3(CH_{2}Cl{\text{-}}CH_{2})_{2}S+2H_{3}PO_{3}}}}
- Из тиодигликоля и соляной кислоты:
( H O — C H 2 — C H 2 ) 2 S + 2 H C l → ( C H 2 C l — C H 2 ) 2 S + 2 H 2 O {\displaystyle {\mathsf {(HO{\text{-}}CH_{2}{\text{-}}CH_{2})_{2}S+2HCl\rightarrow (CH_{2}Cl{\text{-}}CH_{2})_{2}S+2H_{2}O}}}
Получение
Иприт получают тремя способами:
- Из этилена и хлоридов серы, например S2Cl2 или SCl2:
2 C H 2 = C H 2 + S C l 2 → ( C H 2 C l — C H 2 ) 2 S {\displaystyle {\mathsf {2CH_{2}{\text{=}}CH_{2}+SCl_{2}\rightarrow (CH_{2}Cl{\text{-}}CH_{2})_{2}S}}}
- Из тиодигликоля S(CH2CH2OH)2 и трихлорида фосфора PCl3:
3 ( H O — C H 2 — C H 2 ) 2 S + 2 P C l 3 → 3 ( C H 2 C l — C H 2 ) 2 S + 2 H 3 P O 3 {\displaystyle {\mathsf {3(HO{\text{-}}CH_{2}{\text{-}}CH_{2})_{2}S+2PCl_{3}\rightarrow 3(CH_{2}Cl{\text{-}}CH_{2})_{2}S+2H_{3}PO_{3}}}}
- Из тиодигликоля и соляной кислоты:
( H O — C H 2 — C H 2 ) 2 S + 2 H C l → ( C H 2 C l — C H 2 ) 2 S + 2 H 2 O {\displaystyle {\mathsf {(HO{\text{-}}CH_{2}{\text{-}}CH_{2})_{2}S+2HCl\rightarrow (CH_{2}Cl{\text{-}}CH_{2})_{2}S+2H_{2}O}}}
Физические свойства[ | ]
Иприт — бесцветная жидкость с запахом чеснока или горчицы. Технический иприт — тёмно-коричневая, почти чёрная жидкость с неприятным запахом. Температура плавления составляет 14,5 °C, температура кипения — 217 °C (с частичным разложением), плотность 1,280 г/см³ (при 15 °C).
Иприт легко растворяется в органических растворителях — галогеноалканах, бензоле, хлорбензоле — столь же хорошо, как и в растительных или животных жирах; растворимость в воде составляет 0,05 %. В то время, как растворимость в абсолютном этаноле выше 16 °C составляет почти 100 %, в 92%-ном этаноле она едва достигает 25 %.
Вследствие некоторой поверхностной активности он уменьшает поверхностное натяжение воды и в небольшой мере растекается по ней тонким слоем, как плёнка масла. В результате добавления 1 % высокомолекулярного амина C22H38O2NH2 растекание иприта по воде увеличивается на 39 %.
Иприт очень медленно гидролизуется водой, скорость гидролиза резко возрастает в присутствии едких щелочей, при нагревании и перемешивании.
Иприт энергично реагирует с хлорирующими и окисляющими агентами. Так как при этом образуются нетоксичные продукты, указанные выше реакции используют для его дегазации. С солями тяжёлых металлов иприт образует комплексные окрашенные соединения; на этом свойстве основано обнаружение иприта.
Химические свойства
Иприт медленно гидролизуется с образованием соляной кислоты и тиодигликолю:
Он слабо растворяется в воде, поэтому может не испытывать гидролиза длительное время. Процесс гидролиза ускоряют повышение температуры и присутствие щелочей.
Одной из важнейших реакции является действие уротропина при гидролиза: продуктом взаимодействия создаваемой соляной кислоты с уротропином является формальдегид, который способствует заживлению ран:
При действии сильных окислителей (перманганата калия, хроматных кислоты, азотной кислоты, гипохлоритов), сульфид окисляется до сульфоксида, а затем — в сульфона:
Несмотря на то, что продукты окисления также являются ядовитыми веществами, этот способ применяется для дегазации, потому как они являются кристаллическими веществами и не оказывают воздействия на кожу.
Подобно другим тиоетерив, иприт способен образовывать с солями металлов сульфониеви соединения. Образуемые комплексы имеют характерную окраску, а иногда и низкую растворимость, поэтому иногда применяются в аналитической химии. Чаще реакция проводится с галогенидами тяжелых металлов: йодидами и хлоридами меди, цинка, титана, платины, ауру:
Химические свойства[ | ]
При обычной температуре иприт представляет собой устойчивое соединение. При нагревании выше 170 °C он разлагается с образованием неприятно пахнущих ядовитых продуктов различного состава. При температуре выше 500 °C происходит полное термическое разложение. Кратковременное нагревание даже выше 300 °C почти не приводит к образованию продуктов разложения, поэтому иприт считается относительно устойчивым к детонации.
По отношению к металлам при обычной температуре иприт инертен, он почти не воздействует на свинец, латунь, цинк, сталь, алюминий; при повышении температуры сталь разрушается. Загрязнённый иприт, содержащий обычно воду и хлористый водород, вызывает коррозию стали. Образующиеся соли железа способствуют коррозии. Из-за выделяющихся газов (водорода, сероводорода, этилена и других продуктов разложения) следует считаться с повышением давления в закрытых ёмкостях, минах, бомбах и контейнерах для перевозки.
Ингибиторы коррозии и антиоксиданты препятствуют разложению при хранении. Такими веществами могут быть, например, галогениды тетраалкиламмония, гексаметилентетрамин, пиридин, пиколин, хинолин и другие органические аминопроизводные.
В организме человека иприт вступает в реакцию алкилирования с NH-группами нуклеотидов, которые входят в состав ДНК. Это способствует образованию сшивок между цепями ДНК, из-за чего данный участок ДНК становится неработоспособным.
[править] Первая помощь при поражении ипритом
Антидота при отравления ипритом не существует. Капли иприта на коже необходимо немедленно промыть с помощью индивидуального противохимического пакета. Глаза и нос следует обильно промыть, а рот и горло прополоскать 2 % раствором питьевой соды или чистой водой. При отравления водой или пищей, зараженной ипритом, вызвать рвоту, а затем ввести кашицу, приготовленную из расчета 25 г активированного угля в 100 мл воды. Язвы, образовавшиеся из-за попадания капель иприта на кожу, следует обработать перманганатом калия (марганцовка KMnO4).
Разновидности и аналоги[ | ]
С названием «иприт» в качестве боевых отравляющих веществ могут употребляться следующие вещества[5][6][7]:
- собственно иприт (сернистый иприт, HS)
- дистиллированный иприт (HD) — бис(2-хлорэтил)сульфид, иприт очищенный от серосодержащих примесей
- Левинштейновский иприт (Agent H) — 70 % дистиллированного иприта + 30% серные примеси
- иприт Зайкова — этилгруппа заменена на пропилгруппу, обладает более высокой летучестью (tплавл. < 0 °С), чем сернистый иприт и применяется при низкой температуре воздуха
- полуторный иприт (Q) — обладает более низкой летучестью (tплавл. = 56,5 °С), чем сернистый иприт и применяется в смеси с ним при высокой температуре воздуха
- кислородный иприт (T) — бис[2-(2-хлороэтилтио)этиловый] эфир, обладает более низкой летучестью (tплавл. = -10 °С), чем сернистый иприт и применяется в смеси с ним при высокой температуре воздуха
- иприт загущенный (W) — смесь сернистого иприта c загустителем (к примеру, полиметилметакрилат с Mr ≈ 50 кДа), также возможно и добавление люизита (L)
- азотистые иприты — 2-хлорзамещённые алкиламины, структурно и отравляющими свойствами сходные с сернистым ипритом
Поражающее действие[ | ]
Формы применения иприта: воздушно-капельный и жидко-капельный. При поражении воздушно-капельным ипритом преимущественно поражаются органы дыхания (ларинго-трахеит, трахео-бронхит, бронхо-пневмония); при поражении жидко-капельным ипритом — кожные проявления (эритема, везикулы, буллы, язва, некрозы).
Канадский солдат после отравления ипритом Изъязвления и отслоение слизистой гортани и трахеи поражённой парами иприта Рисунок лошади поражённой ипритом — в местах поражения выпадение волос, воспаление и глубокие язвы кожи
Иприт воздействует на организм человека несколькими способами:
- разрушение клеточных мембран;
- нарушение обмена углеводов;
- «вырывание» азотистых оснований из ДНК и РНК.
Иприт обладает поражающим действием при любых путях проникновения в организм. Поражения слизистых оболочек глаз, носоглотки и верхних дыхательных путей проявляются даже при незначительных концентрациях иприта. При более высоких концентрациях наряду с местными поражениями происходит общее отравление организма. Иприт имеет скрытый период действия (2—8 часов) и обладает кумулятивностью.
В момент контакта с ипритом раздражение кожи и болевые эффекты отсутствуют. Поражённые ипритом места предрасположены к инфекции. Поражение кожи начинается с покраснения, которое проявляется через 2—6 часов после воздействия иприта. Через сутки на месте покраснения образуются мелкие пузыри, наполненные жёлтой прозрачной жидкостью, в последующем сливающиеся. Через 2—3 дня пузыри лопаются и образуется заживающая только через 20—30 суток язва. Если в язву попадает инфекция, то заживление может затянуться до 2—3 месяцев.
При вдыхании паров или аэрозоля иприта первые признаки поражения проявляются через несколько часов в виде сухости и жжения в носоглотке, затем наступает сильный отёк слизистой оболочки носоглотки, сопровождающийся гнойными выделениями. В тяжёлых случаях развивается воспаление лёгких, смерть наступает на 3—4-й день от удушья.
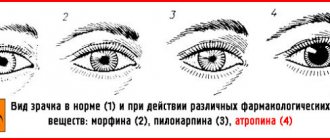
Особенно чувствительны к парам иприта глаза. При воздействии паров иприта на глаза появляется ощущение песка в глазах, слезотечение, светобоязнь, затем происходят покраснение и отёк слизистой оболочки глаз и век, сопровождающийся обильным выделением гноя.
Попадание в глаза капельно-жидкого иприта может привести к слепоте. При попадании иприта в желудочно-кишечный тракт через 30—60 минут появляются резкие боли в желудке, слюнотечение, тошнота, рвота, мелена.
Интересно отметить высказывания В. Мейера (Meyer V.[8]), который получил иприт в чистом виде в 1886 году:
Сначала я склонялся к тому, что явления, наблюдающиеся при действии хлорида, следует объяснить особой восприимчивостью экспериментатора; однако в результате опытов, выполненных по моей просьбе в здешнем физиологическом институте, я уяснил нечто более важное. Согласно этим опытам, это соединение обладает в высокой степени опасными свойствами, как можно было заключить на основании предварительного, ограничивающегося наиболее важными и бросающимися в глаза наблюдениями, сообщения.
Каждого из кроликов средней величины дважды помещали на 3—4 часа в запертую клетку, вентилируемую сильным потоком воздуха. Перед попаданием в клетку поток воздуха проходил через стеклянную трубку, в которой находились полоски фильтровальной бумаги, смоченные 2,2′-дихлордиэтилсульфидом. Животные были возбуждены, часто касались лапами носа и морды, которые имели характерную ярко-красную окраску. Конъюнктива тоже покраснела, а глаза были очень влажными. Выделение влаги кожей заметно увеличилось. На следующий день глаза сильно воспалились, веки склеились гнойными выделениями. Появился сильный насморк, уши сильно опухли, и в слуховом проходе появилось гнойное воспаление. К вечеру третьего дня животные умерли от острой пневмонии, распространившейся на оба лёгких. Один очень сильный кролик, который несколько часов вдыхал пары вещества через отверстие воздуховодной трубки, так что не действовали на поверхность тела, умер уже вечером того же дня от развившейся пневмонии, поэтому времени для проявления других симптомов уже не было.
У кроликов, которым с помощью тонкой кисточки на неповреждённую кожу кончиков ушей было нанесено немного дихлордиэтилсульфида, на месте нанесения совершенно не появилось следов поражения, однако всё ухо сильно опухло, а в одном случае от основания слухового прохода до наружной части уха возникло обильное гнойное воспаление. Возможность затекания препарата в слуховой проход была исключена отчасти из-за незначительности нанесённого кисточкой количества вещества, отчасти вследствие того, что препарат был нанесён на наружную поверхность уха. В случае, когда кожу предварительно обнажали сбриванием шерсти с кончиков ушей, нанесённый кисточкой препарат, разумеется, вызывал преимущественное нагноение в этом месте, но одновременно и более сильное опухание всего уха и воспаление глаз. При подкожном введении примерно двух капель препарата в царапину на коже спины кролика возникало воспаление обоих глаз, очень сильный насморк и на третий день наступала смерть вследствие пневмонии. На месте нанесения препарата никаких признаков поражения не было. Так как пары вещества оказывали на экспериментатора вредное действие, подобное вкратце описанному выше, эти опыты пришлось прекратить.
Минимальная доза, вызывающая образование нарывов на коже, составляет 0,1 мг/см². Лёгкие поражения глаз наступают при концентрации 0,001 мг/л и экспозиции 30 минут. Смертельная доза при действии через кожу 70 мг/кг (скрытый период действия до 12 часов и более). Смертельная концентрация при действии через органы дыхания в течение 1,5 часов — около 0,015 мг/л (скрытый период 4—24 часов).
Первая помощь при поражении ипритом[ | ]
Антидот при отравлении ипритом отсутствует. По опыту врачей Первой мировой войны, первостепенную роль следует отводить первичной санитарной обработке (клиника, как таковая, при поражении ипритом в первые часы после поражения отсутствует). Капли иприта на коже необходимо немедленно продегазировать с помощью индивидуального противохимического пакета. Глаза и нос следует обильно промыть, а рот и горло прополоскать 2 % раствором питьевой соды или чистой водой. Категорически запрещена обработка кожи с помощью растворителей (например, керосином). В связи с высокой растворимостью иприта в органических растворителях, его проникновение в толщу кожи в данном случае будет заметно быстрее, будет быстрее развиваться язвенно-некротическая стадия поражения. При отравлении водой или пищей, заражённой ипритом, вызвать рвоту, а затем ввести кашицу (так называемую «болтушку»), приготовленную из расчёта 25 грамм активированного угля на 100 мл воды. В везикулёзно-буллёзной стадии пузыри следует вскрыть, на место вскрытого пузыря положить повязку, обильно смоченную раствором хлорамина. Язвы, образовавшиеся из-за попадания капель иприта на кожу, следует лечить как ожоги.
Защитные средства[ | ]
Для защиты органов дыхания и кожных покровов от действия иприта используются соответственно противогаз и специальная защитная одежда. Поскольку иприт обладает способностью диффундировать в сложные органические соединения, следует помнить, что ОЗК и противогаз не гарантируют полную защиту кожных покровов. Время нахождения в зоне поражения ипритом не должно превышать 40 минут, во избежание проникновения через средства защиты к коже.
Токсичность
Иприт действует на организм человека или ингаляционная и контактный яд: капли и аэрозоли иприта поражают дыхательные пути, кожу, глаза.
Вещество способно проникать в организм через кожу. Эта способность зависит от температуры окружающей среды: при 21-23 ° C проникновения составляет 1,4 · 10 -3 мг / (см² · мин), при высоких — около 2,7 · 10 -3 мг / (см² · мин). Проникновение в организм иприта в количестве 6 · 10 -3 в половине случаев вызывает появление волдырей. Образование небольших эритем происходит при дозе 0,01 мг / см кожи, крупных — при дозе 0,5 мг / см. Глаза поражаются даже ипритом небольшой концентрации: его действие при концентрации 1,2 · 10 -3 мг / л в течение 45 минут вызывает воспаление глаз, спазмы век, светобоязнь, которые продолжаются до 4 недель.
Действие иприта концентрацией 0,03 мг / л в течение 2-5 минут является летальной. Концентрация 0,01 мг / л опасна в течение 15 минут и ведет к сильным повреждений глаз, кожи.
Контакт иприта за кожей первоначально не вызывает никаких неприятных ощущений. В течение первых 2-5 минут он проникает сквозь кожу, далее растворяется в подкожном жире и впоследствии, через 20-30 минут, полностью всасывается и попадает в кровь. После всасывания наступает скрытый период продолжительностью от 2:00 до суток в зависимости от дозы, температуры и влажности воздуха, структуры и влажности кожи. В жаркую погоду, при горячей, влажной кожи или нежных её участков период скрытого действия значительно сокращается и может быть почти отсутствующим.
Первые признаки поражения после окончания периода скрытого действия проявляются в виде зуда, жжения и покраснения кожи (эритемы) в местах контакта с жидким или газообразным ипритом. Кожа натягивается, становится сухой и теплой. При небольших дозах эти явления через несколько суток проходят. При более высоких дозах развивается отечность, по краям которой через 16-30 часов после контакта с ядом появляется множество мелких пузырьков. В дальнейшем они сливаются в большие или один большой пузырь с бесцветной или желтоватой жидкостью. Пузырьки прорываются и на коже образуются болезненные ипритни язвы, заживление которых может продолжаться более 2 месяцев. Вторичная инфекция может привести к гнойным воспалениям пораженных участков кожи. На их месте остаются рубцы.
Защита
Основной защитой от иприта, в частности, глаз, лица и дыхательных путей, является противогаз. После попадания на хлопчатобумажную одежду иприт за 3:00 полностью пропитывает его, что может в дальнейшем повлечь дополнительные поражения. Для предотвращения попадания соединения на одежду и под него, пользуются специальными защитными костюмами.
Для обработки кожи (устранение незначительных капель иприта), одежды или предметов, которые контактировали с ипритом, применяют окислители и агенты хлорирования (гипохлориты, хлорная известь, хлороамиды).
Примечания[ | ]
- Frederick Guthrie.
XIII.—On some derivatives from the olefines (англ.) // Journal of the Chemical Society (англ.)русск.. — Chemical Society, 1860. — Vol. 12, no. 1. — P. 109—126. — doi:10.1039/QJ8601200109. - Fischer, Karin.
Steinkopf, Georg Wilhelm, in: Sächsische Biografie (нем.) / Schattkowsky, Martina. — Online. — Institut für Sächsische Geschichte und Volkskunde, 2004. - Франке З.
Химия отравляющих веществ. М., «Химия», 1973, т. 1, стр. 136 - Академия ГПС МЧС России Архивная копия от 29 октября 2020 на Wayback Machine
- Классификация отравляющих веществ (ОВ) // Статья в № 3 от 2002 г. журнала «Химическая и биологическая безопасность».
- Термины и понятия, используемые в области химической и биологической безопасности // Статья в № 4-5 от 2002 г. журнала «Химическая и биологическая безопасность».
- Антонов Н. С.
Химическое оружие на рубеже двух столетий / раздел «Основные вехи в развитии химического оружия» // М.: Прогресс. 1994. — 174 с. (С. 28-30). ISBN 01-004462-5. - Meyer V., Chem. Ber., Bd. 19, s. 326 (1886).
Примечания
- Frederick Guthrie.
XIII.—On some derivatives from the olefines (англ.) // Journal of the Chemical Society (англ.)русск.. — Chemical Society, 1860. — Vol. 12, no. 1. — P. 109—126. — doi:10.1039/QJ8601200109. - Fischer, Karin.
Steinkopf, Georg Wilhelm, in: Sächsische Biografie (нем.) / Schattkowsky, Martina. — Online. — Institut für Sächsische Geschichte und Volkskunde, 2004. - Франке З.
Химия отравляющих веществ. М., «Химия», 1973, т. 1, стр. 136 - Академия ГПС МЧС России Архивная копия от 29 октября 2020 на Wayback Machine
- Классификация отравляющих веществ (ОВ) // Статья в № 3 от 2002 г. журнала «Химическая и биологическая безопасность».
- Термины и понятия, используемые в области химической и биологической безопасности // Статья в № 4-5 от 2002 г. журнала «Химическая и биологическая безопасность».
- Антонов Н. С.
Химическое оружие на рубеже двух столетий / раздел «Основные вехи в развитии химического оружия» // М.: Прогресс. 1994. — 174 с. (С. 28-30). ISBN 01-004462-5. - Meyer V., Chem. Ber., Bd. 19, s. 326 (1886).
Литература[ | ]
- Франке З.
Химия отравляющих веществ: В 2-х томах = Lehrbuch der Militarchemie: Band 1, 2 / Зигфрид Франке; Пер. с нем.. — М.: Химия, 1973. — Т. 1. — С. 136—166. — 440 с. - Соборовский Л. З., Эпштейн Г. Ю.
Химия и технология боевых отравляющих веществ / Л. З. Соборовский и Г. Ю. Эпштейн; глава «Дымообразующие вещества» написана Н. И. Мокеевым. — М.; Л.: НКОП СССР. Гос. изд-во оборонной пром-сти, 1938. — 587 с. - Сартори М.
Новое в химии боевых отравляющих веществ / Sartori Mario // Успехи химии. 1954. Т. 21, в. 1. С. 62. - Куценко С. А., Бутомо Н. В., Гребенюк А. Н., Ивницкий Ю. Ю., Мельничук В. П.
Военная токсикология, радиобиология и медицинская защита: Учебник для вузов / Под ред. С. А. Куценко. — СПб.: Фолиант, 2004. — 528 с. — 10 000 экз. — ISBN 5-93929-082-5. - Петренко Э. П.
Военная токсикология, радиобиология и медицинская защита: Учебное пособие. — Саратов, 2007. — 368 с.
Литература
- Франке З.
Химия отравляющих веществ: В 2-х томах = Lehrbuch der Militarchemie: Band 1, 2 / Зигфрид Франке; Пер. с нем.. — М.: Химия, 1973. — Т. 1. — С. 136—166. — 440 с. - Соборовский Л. З., Эпштейн Г. Ю.
Химия и технология боевых отравляющих веществ / Л. З. Соборовский и Г. Ю. Эпштейн; глава «Дымообразующие вещества» написана Н. И. Мокеевым. — М.; Л.: НКОП СССР. Гос. изд-во оборонной пром-сти, 1938. — 587 с. - Сартори М.
Новое в химии боевых отравляющих веществ / Sartori Mario // Успехи химии. 1954. Т. 21, в. 1. С. 62. - Куценко С. А., Бутомо Н. В., Гребенюк А. Н., Ивницкий Ю. Ю., Мельничук В. П.
Военная токсикология, радиобиология и медицинская защита: Учебник для вузов / Под ред. С. А. Куценко. — СПб.: Фолиант, 2004. — 528 с. — 10 000 экз. — ISBN 5-93929-082-5. - Петренко Э. П.
Военная токсикология, радиобиология и медицинская защита: Учебное пособие. — Саратов, 2007. — 368 с.